La variante Omicron del coronavirus 2 del síndrome respiratorio agudo severo (SARS-CoV-2) se detectó inicialmente en Sudáfrica y desde entonces se ha extendido por todo el mundo. La prevalencia generalizada de la variante Omicron se ha relacionado con el rápido aumento en la frecuencia de casos, ya que la investigación actual ha demostrado que las respuestas de anticuerpos neutralizantes se evitan en gran medida contra esta nueva cepa de SARS-CoV-2.
Stady: Pico Omicrónico de SARS-CoV-2 mediado por escape inmunológico, lesión y fusión célula-célula. Haber de imagen: Cryptographer / Shutterstock.com
Conocimientos actuales sobre Omicron
En el Reino Unido, Omicron parece estar compitiendo con la variante Delta previamente dominante. Esto puede deberse a una ventaja tanto en las poblaciones previamente vacunadas como en las expuestas y / o una mayor frecuencia. Sin embargo, hay escasez de información disponible sobre las propiedades de replicación de esta variante.
La proteína pico SARS-CoV-2 Delta tiene una cinética de fusión célula-célula más eficiente en comparación con la cepa de Wuhan de tipo salvaje. Además, la patogenicidad de esta cepa se ha relacionado con cambios en el sitio de escisión de polibase (PBCS). Se predice que la variante Omicron es altamente infecciosa y favorable debido a tres mutaciones en la región del sitio de escisión de la furina que incluyen P681H, H655Y y N679K.
En un estudio reciente publicado en el servidor de preimpresión bioRxiv *, Se encontró que High Omicron se escindió relativamente débilmente y se vio afectado en la mediación de la fusión célula-célula y la formación de sincitios, en contraste con las predicciones basadas en el perfil mutacional de la región PBCS. Esta escisión reducida también se asocia con una entrada deficiente en los orgánulos pulmonares o líneas celulares diana que expresan niveles de autorreceptores.
Además, los autores demuestran que, como era de esperar por el perfil mutacional, la variante Omicron del SARS-CoV-2 tiene una sensibilidad significativamente menor a los anticuerpos neutralizantes y que los sueros de las personas que recibieron la vacuna AstraZeneca (AZ) tenían títulos más bajos en comparación con los que recibieron la vacuna. cualquiera de las vacunas de ARNm. Sin embargo, se puede lograr un título fuerte contra Omicron inmediatamente después de la tercera dosis de la vacuna de ARNm, lo que respalda las estrategias de tercera dosis de ‘refuerzo’.
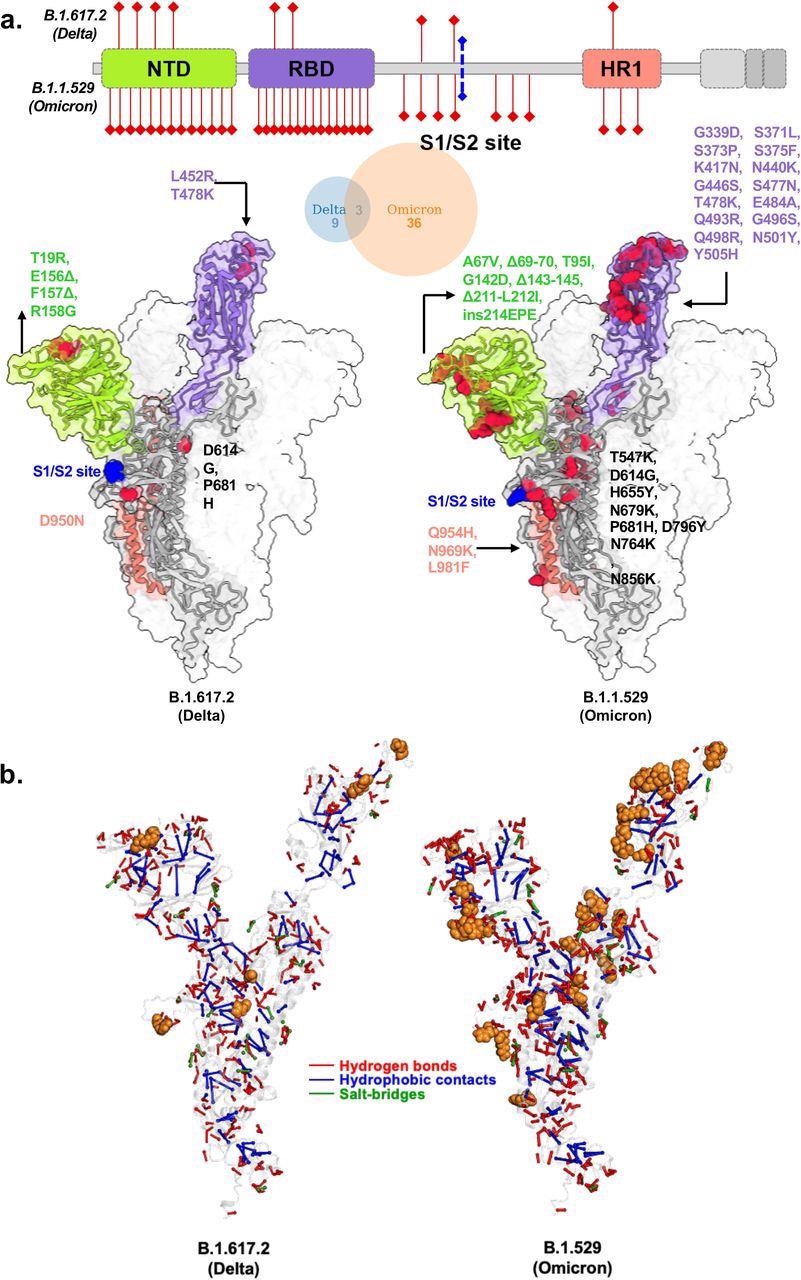
Modelos estructurales de las variantes delta del SARS-CoV-2, pico de Omicron y su correspondiente red proteína-molecular. una. Las estructuras variables del delta y ómicrón de la proteína de pico muestran los sitios de mutaciones en rojo. El diagrama destaca las diferencias en las mutaciones de dominio a lo largo de la proteína. B. Las interacciones no covalentes, incluidos los enlaces de hidrógeno, los contactos hidrófobos y los puentes salinos, se muestran para las variantes delta y omicron en rojo, azul y verde, respectivamente. Las interacciones se calcularon en una simulación de dinámica molecular de 100 ns y las interacciones se muestran con una estabilidad> 50%. Para mayor claridad, los enlaces de hidrógeno únicos de cada proteína de pico variable se resaltan en rojo para una sola cadena. Las mutaciones en delta y omicron están marcadas con.
sobre estudiar
En el estudio actual, los investigadores crearon fotopartículas (PV) sintetizando plásmidos de expresión de picos mejorados por codones para las proteínas de picos Omicron y Delta. Se recolectaron muestras de suero longitudinales de sujetos que habían recibido las vacunas Pfizer-BioNTech BNT162b2 o AZ ChAdOx-1.
En comparación con la variable delta, los autores observaron una pérdida equivalente a diez veces el equivalente de omicron después de la segunda dosis. De hecho, la mayoría de los sujetos que recibieron dos dosis de ChAdOx-1 no tuvieron neutralización Omicron detectable.
Los autores también notan una disminución con el tiempo desde que las vacunas recibieron su segunda dosis. Ambos grupos recibieron una tercera dosis de BNT162b2, lo que permitió realizar comparaciones con la respuesta a esta dosis de refuerzo. Todas las variantes de SARS-CoV-2 probadas mostraron aumentos de magnitud similar en la neutralización, lo que indica una amplitud de respuestas, así como niveles de títulos.
Se han encontrado mutaciones en PBCS en P681 en varias cepas de SARS-CoV-2, más notablemente las variantes Alfa y Delta. Los autores demostraron previamente que estos picos mutantes de p681 tienen un potencial de fusión mucho mayor que el pico D614G de tipo salvaje. En particular, la variante Omicron contiene la mutación P681H, así como las mutaciones 679 y 655.
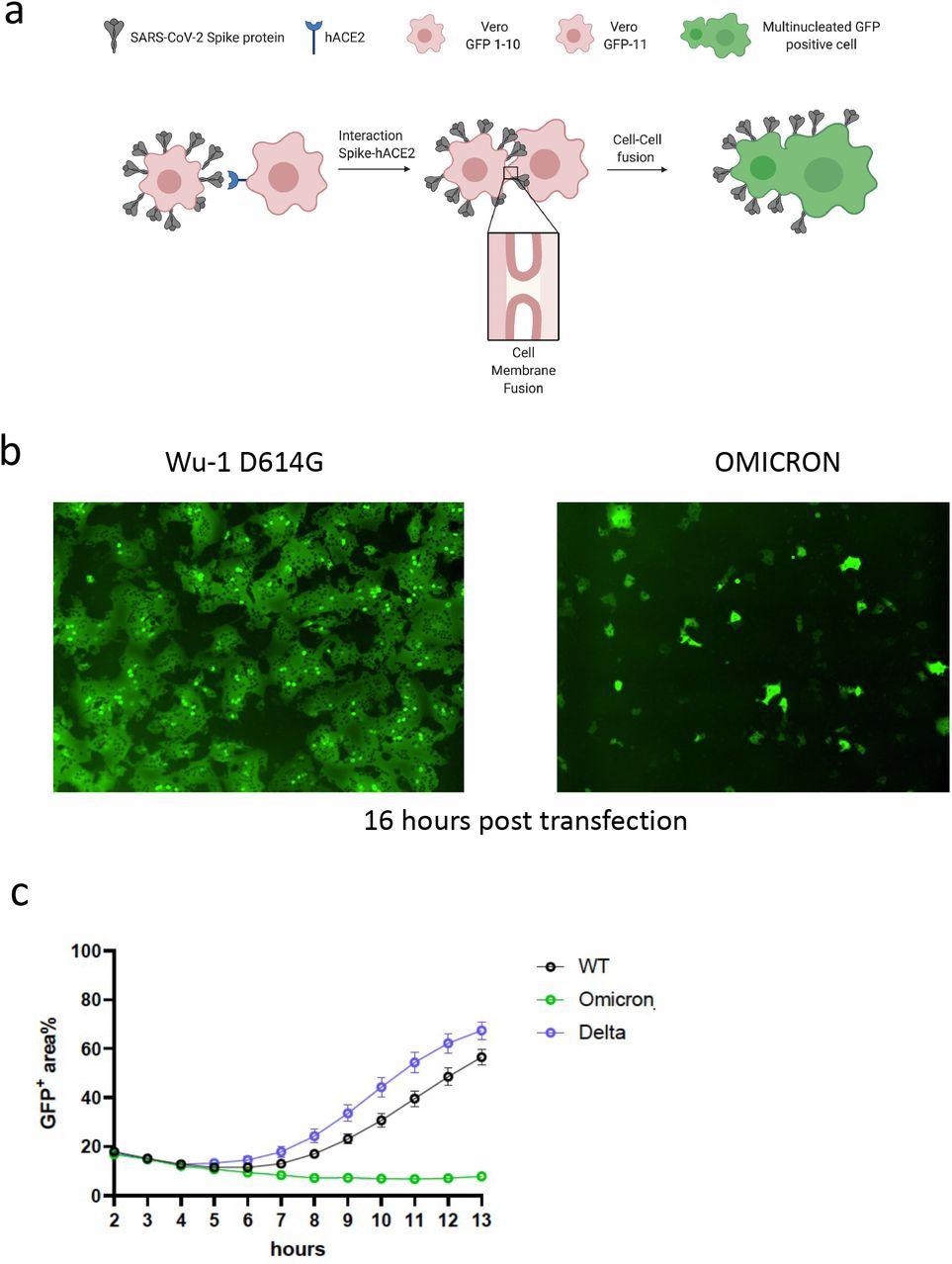
La variante de pico de Omicrón de SARS-CoV-2 imparte una actividad de fusión célula-célula alterada. una. Diagrama esquemático de un ensayo de fusión de citocinas. B. Imágenes reconstruidas a las 16 h de sincitios GFP +. C. Cuantificación de la cinética de fusión célula-célula que muestra el porcentaje de área verde respecto al área celular total a lo largo del tiempo (WT es Wuhan-1 D614G). La media se representa con barras de error que representan el SEM. Los hechos representan al menos dos experimentos independientes.
Los autores utilizaron el sistema de proteína fluorescente verde dividida (GFP) para monitorear la fusión célula-célula en tiempo real durante el ensayo de proteína de pico de Omicron. Los autores transfectaron plásmidos portadores de picos en células 293T que expresan GFP1-10 y se mezclaron con células Vero que expresan de manera estable GFP-11 para permitir la detección y cuantificación de la señal de GFP tras la fusión célula-célula. Los autores observaron un aumento de la fusión de la variante delta en comparación con la anterior elevación de D614G de tipo salvaje. A pesar de su expresividad, la altura de Omicron resultó en una fusión muy débil.
El sistema PV también se utilizó para infectar orgánulos alveolares pulmonares primarios tridimensionales (3D) y células pulmonares Calu-3 que expresan niveles endógenos de la enzima convertidora de angiotensina 2 (ACE2) y la proteasa transmembrana 2 (TMPRSS2), así como el pulmón A549. línea celular transfectada con ACE2 y TMPRSS2. Cuando se seleccionaron los viriones PV en busca de proteína de pico, la proteína de pico de Omicron estaba predominantemente en forma ininterrumpida, lo que contrastaba con las apariencias de la proteína de pico delta y de tipo salvaje.
Los autores descubrieron que la variante Omicron tiene una eficiencia de entrada variable en comparación con Delta y D614G de tipo salvaje. La variante Omicron inhibió la infección por SARS-CoV-2 en organoides y células pulmonares Calu-3 en comparación con Delta y D614G de tipo salvaje. Sorprendentemente, Calu-3 no expresa catepsina L, lo que significa que la entrada depende por completo de la membrana plasmática.
Ramificaciones
Los resultados del estudio actual indican que la variante ómicrón del SARS-CoV-2 adquirió propiedades de evasión inmune al tiempo que altera la formación de sincitios y la entrada de células en las células pulmonares, lo que puede tener efectos patógenos. Fundamentalmente, ChAdOx-1 se usa ampliamente en entornos de bajos ingresos donde faltan terceras dosis de ARNm; Por lo tanto, Omicron puede contribuir a una enfermedad grave en tales condiciones.
*Nota IMPORTANTE
bioRxiv Publica informes científicos preliminares que no han sido revisados por pares y, por lo tanto, no deben considerarse concluyentes, guiar la práctica clínica / comportamiento relacionado con la salud o tratarse como información establecida.






More Stories
El jefe de la Agencia Espacial de EE.UU. quiere hablar con China sobre la basura espacial
Búsqueda de gemas: caracterización de seis planetas gigantes que orbitan enanas frías
La Administración Federal de Aviación de EE. UU. ha puesto en tierra los cohetes Falcon 9 de SpaceX en espera de una investigación sobre un raro accidente de aterrizaje frente a la costa.